对于病理性α突触核蛋白非正常聚集和神经退行性疾病关系的研究
摘要
关键词
α-突触核蛋白;路易小体;神经退行性疾病;
正文
1 引言
神经退行性疾病是一类多发于老年人的神经系统疾病,以其患者脑内神经元非正常死亡而导致身体功能出现障碍为特征。常见的神经退行性疾病有阿尔茨海默症,帕金森综合征,亨廷顿综合征和肌萎缩侧索硬化等。如今,科学家们仍然没有找到彻底治疗神经退行性疾病的方法,临床常见有药物治疗、手术等治疗方式,但都不能彻底治愈。因此寻找神经退行性疾病的病理成因从而寻找新的治疗方式迫在眉睫[1]。
随着研究的深入,科学家们发现帕金森综合征病人脑组织神经元中含有大量的路易小体。路易小体的主要组成部分是不溶性α突触核蛋白纤维。生理状态下,α突触核蛋白(α-Synuclein)是一种可溶性蛋白,其结构可随胞内情况发生改变。在病理状态下,α-syn聚集成不溶性纤维蛋白沉淀[2]。近年来,α-syn成为帕金森综合征的主要研究方向。大量实验证明,病理状态下α-syn异常折叠形成的寡聚体具有很强的神经毒性[3]。这些异常的蛋白可以被其他细胞摄取。这些被吞噬的寡聚体会影响正常α-syn的折叠,在细胞内形成不溶性纤维,进而聚集形成路易小体,阻碍神经元正常发挥生理功能[4],甚至会导致神经元的死亡。
这些以α-syn异常为病理特征的神经退行性疾病被统称为α突触核蛋白病,常见有帕金森综合征、路易体痴呆、多系统萎缩症等。在帕金森综合征中,路易小体沉积在中脑黑质、嗅球、脑干等地,造成运动、嗅觉等身体障碍。在路易体痴呆中,α-syn纤维不仅存在于中脑黑质,同时还累积在边缘系统。而在多系统萎缩中,α-syn纤维被认为影响少突胶质细胞从而导致自主神经功能障碍。
本文旨在调查不溶性α突触核蛋白纤维和神经退行性疾病的关系。运用PD小鼠模型,对其大脑切片进行免疫荧光染色,观察路易小体,证明α突触核蛋白出现病理性聚集是造成神经元死亡的原因。
2 方法与材料
2.1材料
兔源抗磷酸化α-突触核蛋白(P-a-syn),鸡源抗GFP,山羊抗鸡488,山羊抗兔546,PBS(sigma1:200ml),PBST(0.7%TritonX-100溶于PBS),DAPI稀释液,抗荧光淬灭封片剂(Beyotime公司生产),VS120显微镜,Airyscan2公司型号为LSM980激光扫描共聚焦荧光显微镜。
2.2方法
2.2.1 小鼠心脏灌流和取脑
小鼠麻醉后用37摄氏度的生理盐水做心脏灌流。待小鼠血液基本流出后(约8到10分钟),用200毫升4%的多聚甲醛(PFA)溶液固定小鼠蛋白形态。PFA灌流约40分钟后,小鼠四肢僵直,取出小鼠大脑,进行后续切片。
2.2.2 大脑冰冻切片
将取出的小鼠大脑用20毫升的4%的多聚甲醛溶液浸泡6到8小时进行后固定。浸泡结束后将多聚甲醛溶液倒出,用约其体积10倍的30%的蔗糖溶液在4摄氏度的温度下脱水1到2天。待小鼠大脑沉到蔗糖溶液底部后,将大脑取出,从嗅球后修剪平整。竖直放在已经修剪平整的有冰冻组织包埋剂的底座上,再用组织包埋剂冷冻固定。用切片机将小鼠大脑切片保存在装有1XPBS的24孔板里,5片为一单位,4度保存。
2.2.3 免疫荧光染色
挑出需要进行染色的脑片,放入溶解在PBST中10%的山羊血清配制成的封闭液中,在4摄氏度120rpm的摇床上摇过夜。一抗鸡源GFP和兔源抗磷酸化的α突触核蛋白与PBS 1:2000稀释,120rpm的摇床上室温孵育6个小时。用PBST清洗一抗,将脑片室温120rpm摇床上摇10分钟,共三次。二抗山羊抗鸡488和山羊抗兔546与封闭液1:500稀释,将脑片加入二抗稀释液后,在120rpm的摇床上孵育2个小时。随后用PBST清洗二抗。DAPI母液与PBS 1:5000稀释后室温120rpm摇15分钟,然后用PBST进行清洗。最后展片,用抗荧光淬灭封片剂封片。
2.2.4激光扫描共聚焦荧光显微镜扫描
Leica公司型号为VS120的显微镜,放入要扫描的脑片,白光明场预览调整扫描范围后,蓝色荧光预览并调整焦距。聚焦后对脑片DAPI进行扫描。开启LSM980激光扫描共聚焦荧光显微镜,向参数为63xoil的物镜上滴一滴松柏油,将脑片倒置放置在物镜上方,配置光路,设置拍照参数后用物镜观察。在电脑上选择观察视野,用Z-Stack层扫并设置起点和终点、厚度和间距,开始扫描。
3.结果与分析
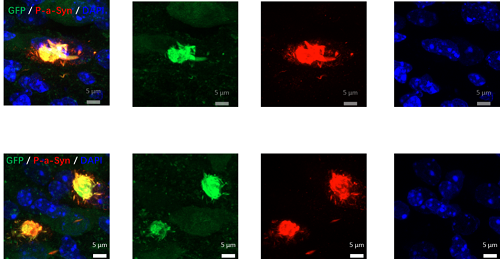
图为基因型为KI-SNCA-GFP+-小鼠DMV脑区切片的荧光染色扫描图像,绿红蓝色荧光分别为GFP、P-a-Syn、DAPI细胞核
如图显示,在迷走神经背运动核(10N脑区)注射了PFF的小鼠(基因型为KI-SNCA-GFP+-)的10N脑区可以观察到明显的点状绿色和红色荧光,分别代表GPF分子和磷酸化α-syn的大量聚集,代表了小鼠脑中的路易小体。在Sangjune Kim等人的研究中,仅注射了PBS小鼠的10N脑区没有明显的路易小体聚集[5],而在被注射PFF的小鼠中可以观察到其10N脑区的病理性α-syn的大量聚集,形态与本次实验类似。以上结果表明PFF可以促进10N脑区路易小体聚集,对该脑区的神经元造成损伤,产生PD相关症状。
在Jessie L. St Martin等人的研究中,他们运用小鼠模型观察到,在病理性α-syn聚集的脑区中,神经细胞大量丢失,认为病理性α-syn的聚集纤维会导致神经元和胶质细胞的死亡[6]。基于此我们可以推断,路易小体会造成神经元的死亡,不同脑区神经元的死亡会产生多种身体功能障碍,引发不同特征的神经退行性疾病。
4.讨论与结论
后续的研究中,本实验预计增加对照组观察正常小鼠的10N脑区切片,并进行多次重复实验。我们本次在PFF注射后4个月进行小鼠脑片观察,PFF扩散时间不长,因此路易小体尚未完全成熟、传播,所以仅局限于10N脑区,可能因存在一定的误差。所以,在之后的实验中,我们可以适当延长注射后观察时间,设置时间梯度对照。
神经退行性疾病作为中老年人中常见的神经系统疾病,严重损害中老年人的身体健康和晚年的幸福生活。目前神经退行性疾病的主要治疗手段是通过药物治疗或手术,但不同神经退行性疾病中造成神经元损伤的物质、被损害的区域等各不相同,尚未存在有效的干预措施抑制大脑中有害物质的合成。路易小体作为能够损害神经元和胶质细胞的有毒物质,其主要组成部分α-syn纤维具有神经毒性。因此,研发出预防或抑制α-syn纤维化聚集药物将极大程度预防或提高患者生活质量,减少其不良生理反应对正常生活产生的影响。
参考文献
[1] 薛小燕,郭小华,李敏,罗焕敏.神经退行性疾病发病机制研究进展[J].中国老年学杂志,2015(11):3149-3152
[2] 王丹晨,于珊珊,刘巍峰,陈冠军.α-Synuclein蛋白聚集状态与帕金森病形成[J].中国生物化学与分子生物学报,2006(8):615-620
[3] 钱小娟,刘娜,张杨,杨心玲.病理性α-突触核蛋白跨细胞传播和研究进展[J].卒中与神经疾病.2022.4(29.2):189-194
[4] 毛婷婷,陈煜森.α-突触核蛋白在帕金森病发病机制中的研究进展[J].海南医学.2020.6(31.11):1460-1463
[5] Sangjune Kim et.al. Transneuronal Propagation of Pathologic α-Synuclein from the Gut to the Brain Models Parkinson’s Disease[J].Neuron.2019.8(103.4): 627-641.e7
[6] Jessie L. St Martin et.al. Dopaminergic neuron loss and up-regulation of chaperone protein mRNA induced by targeted over-expression of alpha-synuclein in mouse substantia nigra[J].Journal of Neurochemistry.2006.11(100.6):1449-1457
...