农作物对重金属镉抗性的多组学研究进展
摘要
关键词
农作物; 镉; 多组学
正文
前言:在植物中,镉作为非必需生长元素,不会被利用,易在植物体内富集,并对植物产生伤害。此外,植物通过根吸收土壤中的镉离子,再经由木质部和韧皮部向植物体内各器官进行输送和转运,最后可大量留存于茎、叶和籽粒中,从而对食用者造成伤害。因具有相对较长的生物半衰期和很低的排泄率,镉极易经由食物链摄入人体内。主要危害包括通过氧化应激对人体的肝、肾、骨、神经系统等造成损伤,可以造成骨代谢混乱,骨痛病等(Ma et al.,2022)。此外,还对男女性的生殖能力有着一定程度的损伤,造成不孕(Lee, Min and Min, 2020)。镉甚至还会引起心肌细胞内质网应激和能量受损,对心血管系统也有相当程度的危害(Chen et al., 2015)。因此,研究农作物对重金属镉的吸收、富集、积累和转运有重要意义。
随着科学技术的快速发展,我们对植物镉胁迫的耐受、转运、作用机理等有了更深入和全面的研究。近些年,结合“多组学”研究可以从整体水平上对机体的生命活动规律进行分析,可以更好的突破单一组学的局限性。随着多种组学技术的发展,我们可以更准确和详细的分析植物对重金属镉毒性的响应机理。因此,多组学技术是未来研究农作物对重金属镉胁迫的重要方向,为快速探索镉在植物体内的富集、积累、调控和转运提供信息。上述研究与人类的生命健康和福祉息息相关,是未来研究的主要趋势。如图一,展现了多组学分析技术在农作物抗镉方面的应用。
1本文综述了近5年来,主要农作物包括水稻、大麦、小麦、油菜和大豆等对镉吸收、富集、积累和转运的研究,结合基因组学、转录组学、蛋白组学、代谢组学等方面的研究进展。并对近9年国内外发表的相关论文进行可视化分析,(如下图2所示)进一步说明多组学整合在作物镉胁迫领域的应用。图2通过citespace文献分析软件,将2014–2023年间国内外对农作物镉抗性研究的论文进行了可视化分析。英文数据来源于Web of ScienceTM核心集合,中文数据来源于中国知网(CNKI,China National Knowledge Infrastructure)数据库。时间切片为1年,节点类型为关键词(keyword)。经关键词共现图可见,“转录组学”、“代谢组学”、“蛋白组学”、“抗性机制”是中国知网CNKI的高频关键词,表明了他们在作物受镉胁迫下具有重要的调控关系。据时间点的区域颜色可见,2014-2023年间出现了大量相关的突现词和关键词,表明组学技术成为研究作物镉胁迫的热点,随着关键词的增加,研究领域也在不断拓展。
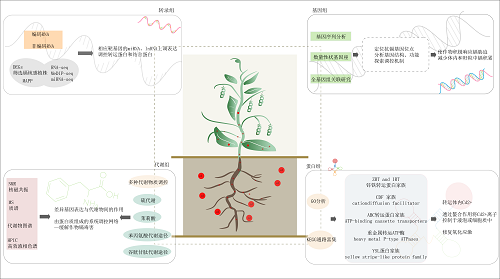
图1:多组学揭示了镉胁迫下的作物作用机制。
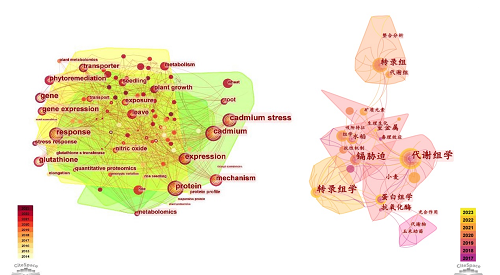
图2:2014–2023年国内外相关研究论文关键词共现图。左侧为2014–2023年Web of ScienceTM核心集数据。图右侧部分为中国知网核心数据库。
1.基因组学
1986年,美国遗传学家Thomas H.Roderick首次提出了基因组学的概念,基因组学也被定义为主要研究基因组的结构、功能、进化、定位和编辑等,以及对生物的影响。确定基因和性状间的关系是基因组研究的重要内容。目前已有多种性状定位方法,主要包括QTL(Quantitative trait locus,数量性状基因座)定位和GWAS(Genome-Wide Association Studies,全基因组关联研究)关联分析。表一汇总了小麦、大麦、水稻等主要响应镉基因的相关研究。
1.1 QTL定位
QTL定位是指数量性状位点定位。通过使用遗传标记分析遗传连锁群,将一个或多个QTL定位到位于同一染色体的遗传标记旁,快速定位相关性状的候选基因。在农作物对镉胁迫响应的研究中,QTL定位被广泛应用于快速发现Cd耐性基因。Derakhshani等人在大麦2H染色体和6H染色体上各检测到Cd胁迫下表达黄萎病和坏死性状的主要QTL位点(Derakhshani et al.,2020)。对大豆低镉QTL进行研究,在X4050(大豆种类)群体中鉴定出7个与Cd积累相关的基因(Nissan et al.,2022)。在水稻籽粒镉积累研究中,鉴定到11个主效低镉积累QTL、2个新的低镉积累QTL位点(王,2020)。上述研究表明在农作物中都定位到了多个镉胁迫相关QTL,为抗镉农作物筛选打下了坚实基础。
1.2 GWAS关联分析
GWAS全基因组关联分析,是现阶段使用最多的性状定位手段。一般应用于自然群体上的全基因组范围内多性状定位及目标性状的生物学基础研究。GWAS克服了传统QTL性状定位的许多限制,提高了结果的精确度,能将多个个体的特定基因变异与特定性状联系起来。在一项水稻GWAS研究中,鉴定出35个与Cd积累显著相关的QTL,其中仅检测到qCd8-1(Pan et al.,2020)。并发现基因OsABCB24可能是与Cd积累量低相关—qCd1-3的候选基因(Pan et al.,2020)。最近一项小麦GWAS研究中分析得出179个关联SNPs(Safdar et al.,2020a)。这些位点中与籽粒中镉积累有关的基因为qSCd-1A和qSCd-1D(Safdar et al.,2020a)。通过对油菜60K SNP分析,检测到根和地上部Cd积累和Cd易位的多个QTL,共包含98个单核苷酸多态性(SNPs)(L.Chen et al.,2018)。且检测出抗镉相关的候选基因:IRT1、NRAMP6、PCS1、PCS2和GSTs,经验证与拟兰芥同源(L.Chen et al.,2018)。
植物种类 | 染色体位置(chr) | 基因距离(cM) | 名称 | 功能 | 主要抗镉基因 | 备注 | 参考文献 |
大麦 | 2H | 147.1 cM | 8586-1221 | 籽粒中镉积累 | 主效QTL | (Wu, Sato and Ma, 2015) | |
5H | 2.81 cM | / | 与镉胁迫下调节株高相关 | / | (Wang et al., 2019) | ||
5H | 132.6cM | ABC04322-1-3-208 | 地下部到地上部的cd的易位 | 主效QTL | (Wu, Sato and Ma, 2015) | ||
6H | 55137978-55142780 | PF03109.15 | ABC转运蛋白的表达 | ABC家族基因 | 主效QTL | (Derakhshani et al., 2020) | |
7H | TP18054和TP11089之间的2.6cM区域 | qShCd7H | 与cd浓度相关、主要调节cd浓度、表达时可使地上部cd浓度降低 | HvPAA1 | 主效QTL | (Wang et al., 2019) | |
水稻 | 1H | / | qCd1-3 | 实现水稻籽粒中低镉积累 | OsABCB24 | / | (Pan et al., 2020) |
2H | 未克隆 | qGCd2 | 实现水稻籽粒中低镉积累 | 小效QTL | (Ishikawa et al., 2010) | ||
7H | 7.23-7.61 Mbp
| qGCd7 | 实现水稻籽粒中低镉积累 | OsHMA3/OsNramp1/OsNramp5 | 微效QTL | (王, 2020) | |
13H | / | qLCdG3/qCd-3-2 | 实现水稻籽粒中低镉积累 | OsHB4/OsCCX2/OsCDT1/OsIRT1/ | / | (Guo et al., 2019) | |
5H | 4.20–6.33 | qBRCdC-5 | 与重金属转运和谷胱甘肽转移酶相关 | 主效QTL | (Guo et al., 2019) | ||
9H | 21.27–22.35 | qBRCdC9 | 与重金属转运和谷胱甘肽转移酶相关 | (Guo et al., 2019) | |||
12H | 3.05–3.33 | qBRCdC-12 | 与重金属转运和谷胱甘肽转移酶相关 | (Guo et al., 2019) | |||
小麦 | 1A | 462435832 bp | qSCd-1A | 与镉转运蛋白相关 | (Safdar et al., 2020b) | ||
1D | 14985862 bp | qSCd-1D | 与镉转运蛋白相关 | / | (Safdar et al., 2020b) | ||
5B | 81.27–90.71 | QCd.uia2-5B | 控制小麦籽粒Cd含量使其低积累 | TaHMA3 | 主效QTL | (Qiao et al., 2021) | |
7B | 153.22–159.88 | QCd.uia2-7B | 控制小麦籽粒Cd含量使其低积累 | TaHMA2 | 主效QTL | (Qiao et al., 2021) | |
7D | 40.26–49.88 | QCd.uia2-7D | 控制小麦籽粒Cd含量使其低积累 | / | / | (Qiao et al., 2021) | |
5B长臂 | 4.27 Mb | Cdu-B1 | 二价金属蛋白结合进行转移 | TdHMA3-B1 | 主效QTL | (Maccaferri et al., 2019) |
2转录组学
转录组学是指从RNA水平来研究基因表达情况的一门技术。转录组这个概念最初由Velcuescu(Velculescu et al., 1997)等在研究酵母基因表达时提出。当前主要通过高通量测序技术对组织或细胞中所有RNA进行测序,统计其相关Reads数,分析转录本的结构和表达水平。因此通过设计差异比较组合寻找差异基因和富集通路,可以快速预测出对应变化的靶基因位点和响应的调控通路等。
利用RNA-seq技术快速分析受镉胁迫下不同耐镉品种农作物间RNA上调、下调表达,从而快速筛选抗镉基因和分子调控机制。Yu等人比较了具有Cd抗性的野生WB-1大麦和栽培大麦,发现野生WB-1对Cd响应的基因为miR156、miR159、miR166、miR167、miR171和miR393(Yu et al.,2019)。Zhou等人比较了两种大麦不耐镉和耐镉基因型W6nk2和ZN8对Cd胁迫响应的lncRNA转录组,并在ZN8(耐镉基因型)中鉴定了21个与Cd耐受相关的lncRNA。发现靶基因HvGAMYB在调控Cd胁迫耐受中发挥了积极作用(Zhou et al.,2023)。对番茄转录的研究,发现miR398的下调在番茄镉胁迫中发挥了保护作用(Yan et al., 2023)。
转录组测序还可以通过KEGG通路分析、qRT-PCR(Quantitative Real-time PCR)等方法分析靶基因对应的调控镉响应通路。利用RNA测序分析显示表达于叶片花朵中的GmWRKY172基因在抗镉大豆中调控了镉逆境相关的途径(Xian et al.,2023)。对糯玉米镉响应不同时间点下KEGG分析表示,耐镉品种N46富集显著的通路有ABC转运蛋白、黄酮类、氨基酸类生物合成以及氨酰-tRNA生物合成(张,2020)。并通过比较耐镉材料N46和镉敏感N28基因Zm00001d045375和Zm00001d012498在两个时间点与蛋氨酸的关系分析出其该基因通路与玉米耐镉调控有密切联系(张,2020)。对油菜miRNA测序发现,miR169n、miR161、miR860和miR6034表达上调,而miR6030表达下调。结合qRT-PCR验证表明,miRNAs参与了甘蓝型油菜对Cd胁迫的生物胁迫防御、离子稳态和次生代谢合成的调控(Jian et al.,2018)。
3.蛋白质组学
蛋白组学主要以全蛋白组(组织、细胞和器官)为研究对象,通过对蛋白组进行定性、定量、分子功能、通路互作和蛋白互作分析,揭示生物学功能、作用机制、及预测蛋白的上、下游变化关系,是研究基因组与表型之间的桥梁。现阶段已有诸多研究表明多种蛋白质在Cd胁迫下帮助植物实现转运、降低关键部位镉浓度、控制镉转运等。
3.1螯合作用:
植物螯合作用是植物生长发育的重要机制之一。植物螯合肽(PC,Phytochelatin)和金属硫蛋白(MT,Metallothionein)是镉的天然配体,能与镉进行螯合,形成螯合物。通过转运体将螯合物转移至液泡中,缓解镉对植物的毒害作用。植物螯合肽在低重金属浓度下无明显表达,当重金属浓度升高到一定程度时,GSH被消耗合成大量PC(Grill et al.,1989)。此时Cd2+与PCs结合形成低分子量化合物,在HMT1膜转运体的作用下,进入液泡,以实现控制镉毒性的作用。金属硫蛋白(MT)是一种低分子、富含半胱氨酸短肽、具有金属结合能力和高诱导特性的一类蛋白质分子,对多种重金属具有高度亲和性。在对甘蓝(Brassica parachinensis L.)结合镉蛋白研究中发现,Cd胁迫下CX4中巯基(PC2和PC3)增加,且参与Cd在根中的高积累和Cd-pc复合体的根到枝转运(Fu et al.,2020)。水稻幼苗镉毒害响应中发现其体内通过加强诱导合成谷胱甘肽(GSH)、植物螯合肽(PCs)和金属硫蛋白(MT)等巯基化合物来应对缓解毒害作用。并且外源适当添加S(Sulphur,硫)、Se(Selenium,硒)可以促进巯基物质生成,增加了螯合作用以此缓解胁迫(张,2014)。在对玉米的金属硫蛋白基因家族研究中,分析了ZmMT蛋白主要结构和对重金属尤其是Cd胁迫下有着重要的结合作用:大都含有一个高度保守的金属硫氧结构域,其中ZmMT4含有一个金属硫氧_PEC结构域(Gao et al.,2022)。
3.2转运蛋白
Cd2+作为植物体内非必需离子,体内没有特定的转运载体。其转运主要通过二价金属离子的转运蛋白如Zn2+、Fe2+金属离子蛋白和多种载体蛋白来实现。转运途径主要把细胞体内游离的Cd2+转运到液泡中进行隔离、或进行不同部位的转运减少主要器官的富集损伤,以此降低对植物的毒性。OsPT1编码的水稻磷酸盐(Pi)转运蛋白,主要分布在细胞质膜上,可通过其磷酸化位点来影响水稻体内耐镉能力(姜et al.,2023)。在硬粒小麦根中,发现了小麦根系的编码烟草胺合酶蛋白在镉胁迫下上调,其主要机制由于胁迫下NAM(Niacinamide,烟酰胺)增加且上调了两种转运蛋白,即YSL蛋白家族:YSL1(AT4G24120)和YSL2(AT5G24380),位于液泡膜上,能够转运金属-烟胺(NA)复合物(Aprile et al.,2018)。对于花生根部受镉胁迫下的差异蛋白分析找寻到其体内相关镉转运蛋白:ABC蛋白家族包括上调表达、Ca2+-ATPase4、Ca2+-ATPase8、V-型质子atp酶(V-ATPase)等表达上调(Yu et al.,2019)。还在马铃薯中发现了隶属于阳离子转运蛋白家族(CDF)的金属耐受蛋白StMTPs,验证了其参与了Cd转运并其中StMTP5可能也具有将重金属转运至高尔基体外排至细胞外的功能(李,2022)。
4代谢组学
代谢组学是在后基因组学时代兴起的一门跨领域学科,其主要目标是定量研究生命体对外界刺激、以及本身基因突变而产生的其体内代谢物水平的多元动态反应。在过去20年,由于植物结构分析、分离技术的快速发展,为代谢组学的研究提供了一个有利平台(Borges et al., 2021)。
植物受非生物胁迫时,包括有害镉胁迫下会经历代谢紊乱。故对这些代谢特征的分析,可以为植物在生化水平上减轻镉胁迫影响或探究镉毒害机理提供一个新的概述。在对芥菜根响应镉胁迫的代谢研究中,发现不同时期Cd胁迫诱导的芥菜根中氨基酸、有机酸、碳水化合物、脂类、黄酮类、生物碱和吲哚含量存在显著差异(Tan et al.,2021)。且机体通过调节氨基酸、氨基酸-tRNA生物合成、亚油酸代谢、甘油磷脂代谢、ABC转运体、缬氨酸、亮氨酸和异亮氨酸生物合成以及α-亚麻酸代谢来抵抗短效(48h)Cd胁迫。通过调节α-亚麻酸代谢、甘油磷脂代谢、ABC转运体和亚油酸代谢来抵抗长效(7d)Cd胁迫(Tan et al.,2021)。这一相似的代谢途径在籼稻受镉胁迫下同样有所体现:受镉胁迫下水稻籽粒中氨基酸和碳水化合物都呈现下调,其体内有机酸被激活主要采用α-亚麻酸代谢和茉莉酸产生途径来抵御胁迫(Zeng et al.,2021)。
总结和展望
综上,目前重金属污染已经成为了人们不可忽视,着力解决的重要问题。长期镉污染不仅对作物的生长发育、品质和产量有严重影响,更会对人类造成不可逆转的健康损伤。当今对农作物的镉吸收、转运、耐镉机理等都取得了重大进展。随着科技技术不断发展下和各种测序手段不断完善,利用基因组、转录组、蛋白组、代谢组等多组学手段全面分析农作物耐镉胁迫提供了强有力的技术支撑。对于农作物基因组的分析可以快速找到镉响应基因,为培育低镉低积累量的作物奠定了基础。而转录组、蛋白组等是基因表达的产物,代谢组则是蛋白组运作的网络。故多组学的结合,可以将小网络结合成为一个可以覆盖整个机体的巨型大网,让原本隐藏在机体内部的“不为人知”的作用机理彻底展现于研究者的面前。然而,在多组学运用和强大发展的未来,样本数量和数据的大量呈现会带来很多复杂的问题。研究者们过度依靠便捷的组学技术忽略了最基本的探究能力等问题。如何能在浩如烟海的数据中筛选出核心并加以验证、如何正确使用这一强大的工具,需要研究者们强大的分析整合数据的能力、实验思索能力及多种计算机软件的支撑。在未来的探索阶段,多组学会彻底驱散植物Cd胁迫下作用机制的这团迷雾。为选育低镉积累作物、镉污染的治理奠定了基础,还为中国作物安全生产的光明前景开辟了一条新道路。
参考文献
[1]姜南等.(2023)镉胁迫下水稻OsPT1的表达及功能分析,生物技术通报,39(1),pp.166–174..
[2]张金钰(2020)糯玉米苗期镉胁迫下转录组和代谢组分析.硕士.仲恺农业工程学院.
[3]张雯(2014)硫硒交互对水稻幼苗镉累积和毒害的影响机制研究.博士.华东理工大学.
[4]李丹丹(2022)马铃薯金属耐受蛋白(StMTPs)核心特征分析及StMTP8耐镉功能验证.硕士.贵州大学.
[5]王淦(2020)基于SSSL的水稻籽粒镉积累QTL分析与应用.硕士.华南农业大学.
[6]Chen,K.et al.(2018)The miRNAome of ramie(Boehmeria nivea L.):identification,expression,and potential roles of novel microRNAs in regulation of cadmium stress response,BMC Plant Biology,18(1),p.369.
[7]Chen,L.et al.(2018)Genome-Wide Association Study of Cadmium Accumulation at the Seedling Stage in Rapeseed(Brassica napus L.),Frontiers in Plant Science,9,p.375.
[8]Derakhshani,B.et al.(2020)Combined QTL mapping and RNA-Seq profiling reveals candidate genes associated with cadmium tolerance in barley,Plos One,15(4),p.e0230820.
[9]Fu,H.et al.(2020)Screening of the proteins related to the cultivar-dependent cadmium accumulation of Brassica parachinensis L.,Ecotoxicology and Environmental Safety,188,p.109858.
[10]Gao,C.et al.(2022)Genome-wide analysis of metallothionein gene family in maize to reveal its role in development and stress resistance to heavy metal’,Biological Research,55,p.1.
[11]Grill,E.et al.(1989)Phytochelatins,the heavy-metal-binding peptides of plants,are synthesized from glutathione by a specific gamma-glutamylcysteine dipeptidyl transpeptidase(phytochelatin synthase),Proceedings of the National Academy of Sciences of the United States of America,86(18),pp.6838–6842.
[12]Guo,J.et al.(2019a)Genetic properties of cadmium translocation from straw to brown rice in low-grain cadmium rice(Oryza sativa L.)line,Ecotoxicology and Environmental Safety,182,p.109422.
[13]Hirata,K.et al.(2019)Isolation and characterization of induced mutants in the gene associated with seed cadmium accumulation in soybean,Breeding Science,69(2),pp.345–351.
[14]Ishikawa,S.et al.(2010)A major quantitative trait locus for increasing cadmium-specific concentration in rice grain is located on the short arm of chromosome 7,Journal of Experimental Botany,61(3),pp.923–934.
[15]Jian,H.et al.(2018)Genome-Wide Identification of MicroRNAs in Response to Cadmium Stress in Oilseed Rape(Brassica napus L.)Using High-Throughput Sequencing,International Journal of Molecular Sciences,19(5),p.1431.
[16]Lee,S.,Min,J.and Min,K.(2020)Female Infertility Associated with Blood Lead and Cadmium Levels,International Journal of Environmental Research and Public Health,17(5),p.1794.
[17]Liu,X.et al.(2022)TaSWEET14 confers low cadmium accumulation in wheat and is regulated by TaMYB41,Environmental and Experimental Botany,201,p.104992.
[18]Ma Y,Su Q,Yue C, et al.The Effect of Oxidative Stress-Induced Autophagy by Cadmium Exposure in Kidney,Liver,and Bone Damage,and Neurotoxicity[J].International Journal of Molecular Sciences,2022,23(21):13491.
[19]Maccaferri,M.et al.(2019)Durum wheat genome highlights past domestication signatures and future improvement targets,Nature Genetics,51(5),pp.885-+.
[20]Nissan,N.et al.(2022)Novel QTL for Low Seed Cadmium Accumulation in Soybean,Plants-Basel,11(9),p.1146.
[21]Pan,X.et al.(2020)QTL mapping and candidate gene analysis of cadmium accumulation in polished rice by genome-wide association study,Scientific Reports,10(1),p.11791.
[22]Qiao,K.et al.(2019)Effects of cadmium toxicity on diploid wheat(Triticum urartu)and the molecular mechanism of the cadmium response,Journal of Hazardous Materials,374,pp.1–10.
[23]Qiao,L.et al.(2021)Novel Quantitative Trait Loci for Grain Cadmium Content Identified in Hard White Spring Wheat,Frontiers in Plant Science,12,p.756741.
[24]Safdar,L.B.et al.(2020a)Genome‐wide association study identifies five new cadmium uptake loci in wheat,The Plant Genome,13(2).
[25]Tan,P.et al.(2021)Metabolic Profiles of Brassica juncea Roots in Response to Cadmium Stress,Metabolites,11(6),p.383.
[26]Wang,X.-K.et al.(2019)HvPAA1 Encodes a P-Type ATPase,a Novel Gene for Cadmium Accumulation and Tolerance in Barley(Hordeum vulgare L.),International Journal of Molecular Sciences,20(7),p.1732.
[27]Wu,D. et al (2015)Genome‐wide association mapping of cadmium accumulation in different organs of barley,New Phytologist,208(3),pp.817–829.
[28]Xian,P.et al.(2023)Overexpression of GmWRKY172 enhances cadmium tolerance in plants and reduces cadmium accumulation in soybean seeds,Frontiers in Plant Science,14,p.1133892.
[29]Yu,J.et al.(2019)Genotypic difference of cadmium tolerance and the associated microRNAs in wild and cultivated barley,Plant Growth Regulation,87(3),pp.389–401.
[30]Yu,R.et al.(2019)Comparative proteomics analysis of peanut roots reveals differential mechanisms of cadmium detoxification and translocation between two cultivars differing in cadmium accumulation,BMC Plant Biology,19(1),p.137.
[31]Zeng,T.et al.(2021)Mass spectrometry-based metabolomics investigation on two different indica rice grains(Oryza sativa L.)under cadmium stress,Food Chemistry,343,p.128472.
[32]Yan,G.et al.(2023)‘Sly-miR398 Participates in Cadmium Stress Acclimation by Regulating Antioxidant System and Cadmium Transport in Tomato(Solanum lycopersicum)’,International Journal of Molecular Sciences,24(3),p.1953.
[33]Velculescu,V.E.et al.(1997)‘Characterization of the Yeast Transcriptome’,Cell,88(2),pp.243–251.
[34]Borges,R.M.et al.(2021)‘Quantum Chemistry Calculations for Metabolomics:Focus Review’,Chemical Reviews,121(10),pp.5633–5670.
作者简介:姓名:赵小凡,出生年月:(2002年4月— ),性别:女,民族:满族,籍贯:湖南省长沙市芙蓉区东湖街道,学历:本科,研究方向:植物分子生物学
...